¿Cuál es el método de Bradford y el tinte azul de Coomassie?
El Método de Bradford, introducido por Marion McKinley Bradford en 1976, transformó la forma en que se cuantifican las proteínas al incorporar el tinte Azul de Coomassie, ofreciendo un enfoque colorimétrico que se extendió rápidamente por los laboratorios de bioquímica y biología molecular en todo el mundo. Esta técnica gira en torno a la interacción de las proteínas con el tinte Azul de Coomassie, que cambia de color al unirse a las proteínas, facilitando una detección y cuantificación sencilla y precisa de la concentración de proteínas. El método implica una preparación cuidadosa de la muestra, mezcla con el tinte y medición de la absorbancia para correlacionar directamente con la concentración de proteínas.
El uso y las ventajas de este método se extienden a diversas aplicaciones de investigación, convirtiéndolo en una herramienta indispensable para comprender procesos biológicos y el desarrollo de medicamentos. Los detalles detrás del Método de Bradford y el tinte Azul de Coomassie abren una puerta a una comprensión más profunda de experimentos relacionados con proteínas.
Principales puntos a tener en cuenta
- El Método de Bradford cuantifica las concentraciones de proteínas.
- Utiliza tinte azul de Coomassie para el análisis colorimétrico.
- Desarrollado por Marion Bradford en 1976.
- Cuantificación confiable de proteínas en bioquímica.
- Mide el cambio de color inducido por la unión de proteínas.
Resumen del Método de Bradford
La descripción general del Método de Bradford abarca su historia y origen, arrojando luz sobre los principios que sustentan su funcionamiento.
Comprender la evolución de este método, impulsado por Marion McKinley Bradford en 1976, es esencial para comprender su importancia en la cuantificación de concentraciones de proteínas.
Historia y Origen
Originario del año 1976, el Método Bradford, desarrollado por la científica estadounidense Marion Mckinley Bradford, es una técnica espectrométrica notable utilizada para cuantificar la concentración de proteínas dentro de una solución.
- Importancia: El Método Bradford revolucionó la cuantificación de proteínas, ofreciendo una forma rápida y confiable de medir los niveles de proteínas con precisión.
- Innovación: Utilizando el reactivo de Bradford, que contiene tinte azul de Coomassie, el método introdujo un enfoque colorimétrico que simplificó el análisis de proteínas.
- Adopción generalizada: Debido a su simplicidad y efectividad, el Método Bradford rápidamente se convirtió en un procedimiento estándar en laboratorios de bioquímica y biología molecular en todo el mundo.
Principio de Operación
Utilizando un enfoque colorimétrico y técnicas espectrométricas, el Método de Bradford proporciona un medio preciso y eficiente para cuantificar las concentraciones de proteínas dentro de una solución. Este método se basa en la interacción entre las proteínas en una solución y el tinte Azul de Coomassie, que cambia de color según se une a las proteínas. El tinte cambia de rojo a azul a medida que se une a las proteínas, lo que permite detectar fácilmente su presencia.
Lee También
Tinte Azul de Coomassie Explicado
El colorante azul de Coomassie es un componente esencial del Método de Bradford para la cuantificación de proteínas. Este colorante experimenta cambios de color basados en su interacción con las proteínas en una solución, lo que permite la estimación de la concentración de proteínas.
Comprender la estructura química y las propiedades del colorante azul de Coomassie, así como el mecanismo detrás de sus cambios de color, es necesario para la aplicación exitosa del Método de Bradford en la investigación bioquímica.
Estructura y Propiedades Químicas
La estructura química y propiedades del colorante Azul de Coomassie juegan un papel importante en el método de Bradford para cuantificar la concentración de proteínas en una solución. Aquí hay tres puntos clave para entender mejor este colorante:
- El colorante Azul de Coomassie existe en diferentes formas, incluyendo azul aniónico, verde neutro y rojo catiónico, con sus propiedades de cambio de color esenciales para la cuantificación de proteínas.
- La forma catiónica y doble protonada (roja) del colorante se une fuertemente a las proteínas a través de interacciones no covalentes, perturbando el estado normal de las proteínas.
- El cambio de color de rojo (no unido a la proteína) a azul (unido a la proteína) en el colorante se mide a 595 nm, lo que permite la estimación de la concentración de proteínas basada en cambios de absorbancia.
Mecanismo de Cambio de Color
La transformación de color en el método de Bradford, elucidada mediante la aplicación de tinte Azul de Coomassie, es un aspecto clave que facilita la cuantificación de la concentración de proteínas dentro de una solución. El mecanismo implica el cambio de color del tinte Azul de Coomassie basado en su interacción con las proteínas en la solución. A continuación se muestra una tabla que destaca los cambios de color del tinte Azul de Coomassie en diferentes estados:
| Forma de Color | Interacción |
|---|---|
| Aniónico (Azul) | No unido a la proteína |
| Neutro (Verde) | Estado intermedio |
| Catiónico (Rojo) | Unido a la proteína |
| Solución Ácida | Cambio de Rojo a Azul |
Este método colorimétrico se basa en medir la absorbancia de la forma azul del tinte a 595 nm, lo que indica la presencia de proteínas y permite su cuantificación.
Preparándose para un ensayo de Bradford

Para preparar un ensayo de Bradford, los componentes clave incluyen el reactivo de Bradford y los pasos adecuados de preparación de la muestra.
Lee También
El reactivo de Bradford consiste en compuestos químicos específicos que interactúan con proteínas en una solución, lo que permite su cuantificación.
La preparación de la muestra implica asegurar la concentración correcta de proteínas en la solución y seguir pasos precisos para obtener resultados precisos durante el proceso del ensayo.
Componentes del reactivo de Bradford
Los componentes esenciales para la preparación del Reactivo de Bradford, un paso crítico en la realización de un Ensayo de Bradford, implican ingredientes químicos específicos y procedimientos meticulosos.
- Ingredientes Químicos:
- Azul de Coomassie: Un colorante vital para la unión con proteínas en la muestra.
- Etanol: Utilizado para disolver el colorante y crear el reactivo.
- Ácido Fosfórico: Mejora los cambios de color en presencia de proteínas.
- Pasos de Preparación:
- Disolver 100 mg de colorante de Coomassie en 50 ml de etanol al 95% y añadir 100 ml de ácido fosfórico al 85%.
- Una vez disuelto, diluir a 1 litro y filtrar la solución para obtener el reactivo final.
- El reactivo debería verse de color marrón en ausencia de proteínas.
- Significado:
- Los componentes interactúan para producir cambios de color, facilitando la cuantificación de proteínas.
- Una preparación adecuada garantiza resultados precisos en el Ensayo de Bradford.
Pasos de preparación de muestra
En la preparación para un ensayo de Bradford, el paso inicial implica manejar y procesar cuidadosamente las muestras para garantizar una cuantificación precisa de las proteínas utilizando el método de Bradford y el tinte Azul de Coomassie.
En primer lugar, las muestras deben prepararse de manera que asegure que las proteínas no se desnaturalicen o se alteren durante el proceso. Esto incluye condiciones adecuadas de almacenamiento, evitar la contaminación y manipular suavemente para mantener la integridad de las proteínas.
Posteriormente, las muestras deben diluirse a concentraciones apropiadas para el ensayo, típicamente entre 5 a 100 microgramos de proteína por 100 microlitros de solución total.
Lee También Maestría en Mindfulness: Los 12 mejores libros para transformar tu vida
Maestría en Mindfulness: Los 12 mejores libros para transformar tu vidaAsegurar la uniformidad y precisión en la preparación de las muestras es esencial para obtener resultados confiables y reproducibles en la cuantificación de proteínas utilizando el método de Bradford.
Realizando el ensayo
Realizar el ensayo de Bradford implica mezclar las muestras con el tinte Azul de Coomassie y medir la absorbancia de la solución resultante. Este paso es esencial para cuantificar la concentración de proteína presente en las muestras.
Mezclando muestras con tinte
Tras completar la preparación de las muestras, el siguiente paso implica mezclar las muestras con el tinte azul de Coomassie para iniciar el proceso de ensayo. Aquí hay tres pasos clave para contemplar durante esta fase:
- Garantizar una mezcla completa de las muestras y el tinte para promover una distribución uniforme y maximizar la unión del tinte a las proteínas presentes.
- Permitir suficiente tiempo de incubación para que el tinte se una a las proteínas de manera efectiva, típicamente alrededor de 5 minutos, para garantizar resultados precisos.
- Tomar precauciones para prevenir la contaminación durante el proceso de mezcla, ya que cualquier sustancia externa introducida puede interferir con los resultados del ensayo.
Seguir estos pasos diligentemente contribuirá al éxito y la confiabilidad del método de Bradford en la cuantificación precisa de la concentración de proteínas.
Midiendo la absorbancia
Después de mezclar las muestras con el tinte Azul de Coomassie para iniciar el proceso de ensayo, el siguiente paso en el método de Bradford implica medir la absorbancia para cuantificar con precisión la concentración de proteínas. Esta medida es esencial para determinar la cantidad de proteína presente en la muestra.
Al utilizar un espectrofotómetro configurado a una longitud de onda específica, típicamente 595 nm en el caso del ensayo de Bradford, se determina la absorbancia de la muestra. El valor de absorbancia obtenido se correlaciona directamente con la concentración de proteínas, lo que permite la creación de una curva estándar que se puede utilizar para extrapolar la concentración exacta de proteínas en la solución original.
Lee También
Este paso es vital para obtener datos precisos y confiables sobre la concentración de proteínas utilizando el método de Bradford.
Interpretando Resultados
La interpretación de los resultados en el método de Bradford implica comprender las lecturas de absorbancia obtenidas del espectrofotómetro. Estas lecturas correlacionan directamente con la concentración de proteínas en la solución.
Comprendiendo las lecturas de absorbancia
La comprensión de las lecturas de absorbancia es esencial para determinar la concentración de proteínas utilizando el método de Bradford con tinte Azul de Coomassie. Aquí hay tres puntos clave para ayudar a comprender la importancia de las lecturas de absorbancia:
- La absorbancia es una medida de cuánta luz absorbe una sustancia en una longitud de onda específica, con una absorbancia más alta indicando más presencia de la sustancia.
- En el método de Bradford, el cambio de absorbancia de rojo a azul del tinte de Coomassie unido a proteínas se mide a 595 nm, lo que permite la cuantificación de la concentración de proteínas.
- Las lecturas de absorbancia en espectrofotómetros proporcionan una correlación directa con la cantidad de proteína presente en una muestra, facilitando la determinación precisa de la concentración de proteínas.
Creando una Curva Estándar
Para interpretar los resultados obtenidos de las lecturas de absorbancia en el método de Bradford con tinte Azul de Coomassie, se genera una curva pivote para correlacionar los valores de absorbancia con las concentraciones de proteínas. Al trazar concentraciones conocidas de proteínas contra sus valores de absorbancia correspondientes, se establece una relación lineal.
Esta curva pivote sirve como referencia para estimar la concentración de proteínas en muestras desconocidas basándose en sus lecturas de absorbancia. La curva permite una determinación más precisa de los niveles de proteínas en una solución dada, mejorando la fiabilidad del método de Bradford.
Los investigadores pueden extrapolar las concentraciones de proteínas de la curva pivote, lo que permite una cuantificación precisa de las proteínas presentes en diversas muestras biológicas. En última instancia, la curva pivote es una herramienta crítica para interpretar resultados y cuantificar las concentraciones de proteínas de manera efectiva.
Lee También
Ventajas del Método Bradford
El Método de Bradford ofrece varias ventajas clave que lo convierten en una opción popular en la cuantificación de proteínas.
Para empezar, es económico y simple de ejecutar, requiriendo equipos de laboratorio básicos como un espectrofotómetro.
Además, el método es altamente sensible y proporciona resultados rápidos, lo que lo hace eficiente para investigadores que necesitan mediciones rápidas y precisas de la concentración de proteínas.
Eficiencia en costos y simplicidad
El método de Bradford ofrece un enfoque rentable y sencillo para cuantificar las concentraciones de proteínas, lo que lo convierte en una opción favorable en entornos de laboratorio.
Aquí hay tres ventajas clave del método de Bradford:
- Económico: Los materiales necesarios para el método de Bradford son relativamente económicos, especialmente en comparación con otras técnicas de cuantificación de proteínas. Esta asequibilidad lo hace accesible a una amplia gama de laboratorios de investigación con presupuestos variables.
- Fácil de usar: El protocolo del método de Bradford es simple y fácil de seguir, lo que permite a los investigadores obtener mediciones precisas de la concentración de proteínas sin necesidad de una amplia formación o experiencia.
- Eficiente en tiempo: El método de Bradford proporciona resultados rápidos, lo que permite a los investigadores analizar múltiples muestras de manera eficiente, ahorrando tiempo en el flujo de trabajo del laboratorio.
Sensibilidad y Velocidad
Las ventajas del Método de Bradford incluyen su rapidez en la cuantificación de concentraciones de proteínas y su mayor sensibilidad en comparación con otras técnicas de cuantificación de proteínas. La velocidad del método permite un análisis rápido de los niveles de proteínas en las muestras, lo que lo hace eficiente para experimentos de alto rendimiento o investigaciones con restricciones de tiempo.
Lee También
Además, su sensibilidad supera a los métodos tradicionales, lo que permite detectar con precisión concentraciones más bajas de proteínas. Esta sensibilidad es esencial al trabajar con volúmenes de muestra limitados o al analizar soluciones de proteínas diluidas.
Limitaciones y Consideraciones

Al utilizar el método de Bradford, es importante tener en cuenta las posibles limitaciones y los factores que podrían afectar la precisión de las mediciones de concentración de proteínas. Problemas como la interferencia de la muestra, los factores de dilución y la precisión general del método deben ser considerados cuidadosamente.
Comprender estas limitaciones y consideraciones ayudará a los investigadores a garantizar la fiabilidad y validez de sus resultados al utilizar el método de Bradford para la cuantificación de proteínas.
Problemas de interferencia de muestra
En el ámbito de las metodologías de cuantificación de proteínas, se deben tener en cuenta posibles problemas de interferencia en las muestras que pueden influir en las mediciones precisas. Al utilizar el Método de Bradford y el colorante Azul de Coomassie, es importante reconocer los siguientes puntos clave:
- Efectos de la matriz: Varios componentes dentro de la matriz de la muestra pueden interactuar con el colorante, afectando su capacidad de unión a las proteínas y dando lugar a una cuantificación inexacta.
- Interferencias químicas: Ciertas sustancias químicas presentes en la muestra pueden interferir con el desarrollo del color del complejo proteína-colorante, afectando las lecturas de absorbancia y, en consecuencia, los cálculos de concentración de proteínas.
- Interferencias no proteicas: Sustancias distintas a las proteínas que presenten propiedades de absorbancia similares al colorante pueden contribuir a lecturas falsas, complicando la determinación precisa de los niveles de proteínas.
Factores de dilución y precisión
Las consideraciones sobre los factores de dilución y la precisión juegan un papel crucial en la fiabilidad de la cuantificación de proteínas utilizando el Método de Bradford y el Colorante Azul de Coomassie.
Al preparar muestras para el análisis, la dilución adecuada es esencial para garantizar que la concentración de proteínas se encuentre dentro del rango lineal del ensayo, evitando los efectos de saturación que podrían llevar a mediciones inexactas. Los factores de dilución deben calcularse cuidadosamente para lograr los mejores resultados, equilibrando entre la concentración de la muestra y la sensibilidad de detección.
La precisión en la cuantificación de proteínas depende de mantener prácticas de dilución consistentes y registrar con precisión los factores de dilución para asegurar la reproducibilidad. Las desviaciones en las proporciones de dilución pueden introducir errores en los valores finales de concentración de proteínas, resaltando la importancia de un manejo meticuloso y cálculos precisos a lo largo del proceso de cuantificación.
Aplicaciones en Investigación
La cuantificación de proteínas es un aspecto fundamental de la investigación biológica, proporcionando información vital sobre la concentración y presencia de proteínas en diversas muestras.
El Método de Bradford, que utiliza el tinte Azul de Coomassie, desempeña un papel significativo en estudios bioquímicos al permitir a los investigadores medir con precisión las concentraciones de proteínas.
Las aplicaciones de este método en la investigación van más allá de la mera cuantificación, contribuyendo a una comprensión más profunda de los procesos biológicos y ayudando en la evaluación de experimentos relacionados con proteínas.
Cuantificación de proteínas en Biología
Analizar las concentraciones de proteínas juega un papel esencial en diversas aplicaciones de investigación biológica. Aquí hay tres puntos clave a tener en cuenta en el proceso de cuantificación:
- Importancia: La cuantificación precisa de proteínas es vital para comprender los procesos celulares, los mecanismos de enfermedades y el desarrollo de fármacos.
- Metodología: Técnicas como el método de Bradford que utiliza tinte Azul de Coomassie proporcionan un enfoque colorimétrico para medir las concentraciones de proteínas basado en cambios de color, lo que permite a los investigadores estimar el contenido de proteínas en solución.
- Equipos: Al utilizar espectrofotómetros, los investigadores pueden determinar las concentraciones de proteínas al medir la absorbancia a longitudes de onda específicas, ofreciendo un método confiable y ampliamente utilizado en laboratorios para el análisis de proteínas.
Utilización en Estudios Bioquímicos
En la investigación biológica, la utilización del Método de Bradford y el tinte Azul de Coomassie resulta invaluable para cuantificar las concentraciones de proteínas y elucidar procesos celulares esenciales. La naturaleza colorimétrica del Método de Bradford, que se basa en la interacción del tinte Azul de Coomassie con las proteínas, permite a los investigadores medir los cambios de absorbancia, correlacionándolos con las concentraciones de proteínas. Este método ayuda a determinar la cantidad de proteína presente en una muestra, lo cual es importante para diversos estudios bioquímicos. A continuación se muestra una tabla que describe las aplicaciones del Método de Bradford y el tinte Azul de Coomassie en la investigación:
| Aplicación en la Investigación | Descripción | Importancia |
|---|---|---|
| Cuantificación de proteínas | Medir las concentraciones de proteínas en muestras | Importante para comprender los procesos celulares |
| Ensayos de actividad enzimática | Evaluar la función y cinética enzimática | Esencial para estudiar los mecanismos enzimáticos |
| Monitoreo de la purificación de proteínas | Seguir el progreso de la purificación de proteínas | Garantiza proteínas purificadas de alta calidad |
| Ensayos de cribado en el descubrimiento de fármacos | Identificar posibles candidatos a fármacos | Facilita el proceso de desarrollo de fármacos |
| Identificación de biomarcadores | Descubrir biomarcadores para enfermedades | Ayuda en el diagnóstico y tratamiento de enfermedades |
Análisis comparativo
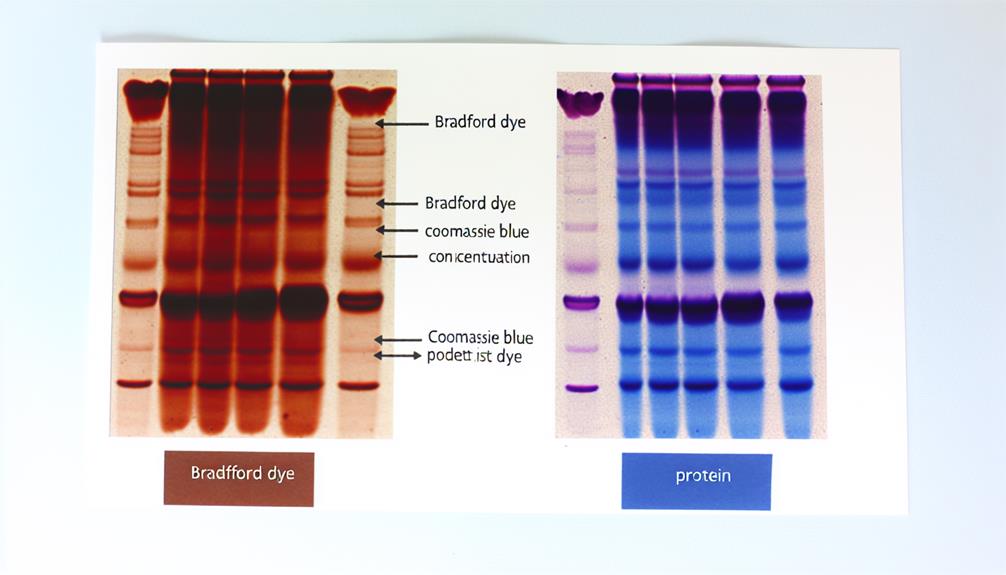
Al comparar el método de Bradford con otros ensayos de proteínas, es esencial tener en cuenta factores como la sensibilidad, la rentabilidad y la facilidad de uso.
Los investigadores deben seleccionar el método adecuado en función de sus necesidades experimentales específicas y de las características de las proteínas que se están analizando.
Bradford vs. Otros ensayos de proteínas
La comparación entre el método de Bradford y otros ensayos de proteínas proporciona información valiosa sobre su eficacia y aplicabilidad respectivas en la cuantificación de proteínas.
- Sensibilidad: El método de Bradford es conocido por su alta sensibilidad, siendo capaz de detectar concentraciones de proteínas en un amplio rango de manera efectiva.
- Velocidad: En comparación con otros ensayos de proteínas, el método de Bradford es relativamente rápido, proporcionando resultados en un tiempo más corto.
- Facilidad de uso: Una de las principales ventajas del método de Bradford es su simplicidad y facilidad de ejecución, lo que lo hace accesible a una amplia gama de investigadores sin necesidad de equipos especializados o experiencia.
Escogiendo el Método Correcto
La selección del método más adecuado para la cuantificación de proteínas implica un análisis comparativo exhaustivo de la sensibilidad, velocidad y facilidad de uso de las técnicas disponibles.
El Método de Bradford, que utiliza el Tinte Azul de Coomassie, ofrece un enfoque colorimétrico sencillo basado en los cambios de absorbancia. Este método es ventajoso debido a su simplicidad y al uso común en entornos de laboratorio.
Al elegir el Método de Bradford, los investigadores se benefician de su facilidad de ejecución y la amplia disponibilidad de espectrofotómetros. Además, la capacidad del método para mejorar la detección de proteínas con niveles bajos de absorbancia, como aquellas que carecen de aminoácidos específicos para mediciones en el rango UV, lo convierte en una elección práctica para la cuantificación de proteínas.
A través de una evaluación sistemática de varios métodos, la selección del Método de Bradford puede agilizar eficientemente la determinación de la concentración de proteínas.
Preguntas frecuentes
¿Se puede utilizar el Método de Bradford para cuantificar proteínas en muestras que no sean soluciones acuosas?
El método de Bradford es principalmente efectivo para cuantificar proteínas en soluciones acuosas debido a su dependencia de las interacciones del tinte Azul de Coomassie. Puede que no proporcione resultados precisos para muestras en entornos no acuosos.
¿Existen interferencias conocidas que puedan afectar la precisión de los resultados del Método de Bradford?
Interferencias como detergentes, agentes reductores y altas concentraciones de sal pueden afectar la precisión del método de Bradford al modificar las interacciones tinte-proteína. Comprender y controlar estas interferencias es esencial para obtener mediciones precisas de la concentración de proteínas utilizando esta técnica espectrofotométrica.
¿Cómo afecta la concentración del colorante azul de Coomassie a la sensibilidad del ensayo de Bradford?
La concentración del colorante azul de Coomassie impacta directamente en la sensibilidad del ensayo de Bradford. Concentraciones más altas de colorante pueden aumentar la sensibilidad, permitiendo una cuantificación de proteínas más precisa. Los mejores niveles de colorante deben determinarse para obtener resultados precisos.
¿Es el Método de Bradford adecuado para cuantificar proteínas con bajas concentraciones en una muestra?
El método de Bradford es adecuado para cuantificar proteínas con bajas concentraciones, ofreciendo un enfoque colorimétrico para determinar los niveles de proteína en una muestra. Al aprovechar las propiedades únicas del colorante azul de Coomassie, este método proporciona mediciones precisas de la concentración de proteínas.
¿Existen otros métodos alternativos al ensayo de Bradford para la cuantificación de proteínas que se utilicen comúnmente en la investigación?
Métodos alternativos al ensayo de Bradford para la cuantificación de proteínas comúnmente utilizados en la investigación incluyen el ensayo de Lowry, el ensayo de BCA y la espectroscopía UV. Estos métodos ofrecen sensibilidades variables, amplios rangos lineales y son adecuados para diferentes tipos de muestras, brindando a los investigadores diversas opciones para la cuantificación de proteínas.
Conclusión
En resumen, el método de Bradford, combinado con el tinte Azul de Coomassie, sirve como una herramienta crucial en la cuantificación de concentraciones de proteínas con precisión y eficiencia.
Al aprovechar los principios colorimétricos y las mediciones espectrofotométricas, los investigadores pueden determinar niveles de proteínas de manera confiable en diversas aplicaciones científicas.
La accesibilidad, confiabilidad y versatilidad del método lo convierten en un activo valioso en el análisis de proteínas, ofreciendo un enfoque estandarizado para medir las concentraciones de proteínas en entornos de investigación y laboratorio.

Deja una respuesta